为了响应内部外部环境变化的要求,各大药企对于研发业务的重视达到了空前的程度,对于研发信息化的探索更是争先恐后。然而,向研发信息化进军是个严肃的话题,因为国内制药企业的产业分布导致了研发信息化方面的基础差、探索不足、差异性不强,对于部分传统型药企来说,这甚至是个相对陌生的领域。不过,我们也看到,部分国内药企对于研发信息化的重视程度高、投入力度大、探索精神强,已经取得了较大的领先优势,为行业整体的研发信息化推进贡献了价值。
5月8日,CIAPH特邀请北京康辰药业股份有限公司信息部总监李博、质量部总监张宇,作客展开群内访谈,从信息化与业务两个视角,为行业同仁分享“康辰药业临床前项目管理系统”。

左:北京康辰药业股份有限公司信息部总监 李博
右:北京康辰药业股份有限公司质量部总监 张宇
以下是访谈内容:
张宇总监:大家好!很高兴能在此与各位同仁共同探讨。
李博总监:下午好!感谢CIAPH给大家搭建的交流平台。在研发信息化方面,康辰药业积累了一些经验,今天分享给大家,同时也有很大的探索空间,希望在接下来的讨论过程中能相互交流,共同学习,共同进步!谢谢大家。
主持人:好的。我们知道,康辰是一家专于研发的药企,请李博总监给大家整体介绍下。
李博总监:好的。北京康辰药业股份有限公司是中国研发驱动型制药企业,成立于2003年,现已成为集高新医药研发、生产、销售于一体的全国性医药公司。
目前,康辰药业拥有国家一类新药苏灵和在研的国家一类新药迪奥、CX1026、CX1003、CX1409等多个创新药组合,并已获得了43项国内、国际PCT发明专利,先后承担并完成了国家863计划、国家火炬计划、国家重大新药创制专项、国家高技术产业化项目。
康辰在创新药研发上聚集起了强劲的核心竞争力,其中,历经十多年研发并成功上市的国家一类新药苏灵,是截至目前世界范围内唯一的高纯度、单组份的注射用血凝酶产品,现已成长为业内领军品牌。苏灵在临床上的广泛应用,为血源和医疗费用有限的中国,贡献了巨大的经济和社会效益。
康辰药业以研发创新为先导,以质量信誉为保障。除此之外,还凭借“联盟营销”模式和独具特色的企业文化体系,成为广受关注和追踪的标杆性案例。
主持人:好的。感谢李总的介绍。康辰对于研发业务的定位很明确,请您介绍下,康辰的研发信息化建设的背景和规划思路。
李博总监:好的,主持人。
为了灵敏及时的应对行业环境变化,康辰公司要求信息部每半年更新一次信息化规划,同时针对不同业务方向单独进行信息化规划。
公司信息化规划思路分为三个层面:设施平台层、信息系统层、决策支持层;信息系统分为两个层次:横向利用ERP等管理系统完成公司人流、物流和信息流的打通,纵向从研、产、销三个业务层面单独规划延伸。
康辰药业是一家以研发创新药为主的公司,因此研发端信息化建设是业务系统建设中的重中之重。
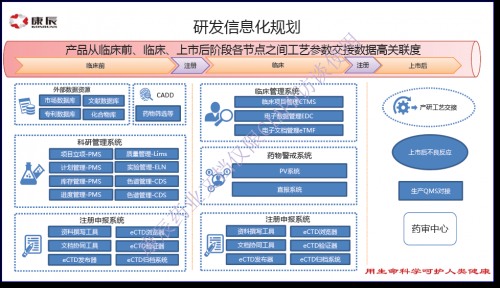
基于QBD的理念,产品质量源于设计,研发阶段的质量管理水平决定了最终产品的质量,规范化的管理、建立并执行良好的研发质量管理体系是优质产品诞生的必要条件。
新药研发周期长,研发难度大,因此每一个优质新药设计都离不开前期大量的研发实验和研发论证,虽然与药品研发相关的过程都遵循《药品非临床试验质量管理规范》、《药物临床研究质量管理规范》等法规要求,但在传统手工管理模式下依然会出现工艺的适用性及重现性差、药品的稳定性得不到保证、试验样品结果达不到预期,研发项目总是延期、项目组成员工作安排不合理等诸多问题,因此通过信息化系统进行管理就显得格外重要。
研发阶段划分为临床前和临床两个阶段,均是以项目为核心进行管理,但是两阶段的侧重点是不同的:临床前阶段以小试、中试、药理毒理等研究为主,侧重实验过程与数据管理;临床阶段管理以临床试验为主,更侧重方案执行与数据稽查。两个阶段管理的维度不同,因此系统架构完全不同,并且关联度不高,两个阶段的系统可单独进行设计和建设,彼此之间通过数据打通关联查询即可。
“722”事件后大多数制药企业在临床阶段的信息系统建设都已接近完毕,主要采用CTMS+EDC的解决方案,因为eCTD的实施以及近两年企业对药物警戒的不断重视,未来临床端解决方案会更多的向三个方向倾斜:
第一,CTMS+EDC+eTMF+PV,CTMS需和临床前项目管理打通,用于项目维度信息关联查询;
第二, 第二种PV更多的要和上市后生产质量QA管理系统QMS打通,质量投诉和药物警戒协同分析;
第三, 文档全生命周期管理,未来更多的药企会重视使用eDMS、eTMF临床试验文档系统和eCTD归档系统。
总体来说临床阶段行业信息化发展比较快,解决方案比较成熟,在此不做过多陈述。本次访谈我重点谈一下康辰药业临床前项目管理系统(后文称为“科研管理系统”)如何选择。
主持人:感谢李总。您刚才的介绍很全面,您也谈到了今天的分享聚焦于临床前项目管理系统,即科研管理系统。我们都知道,信息化建设源于业务的需求,最后实现和满足业务需求,我们今天就按照这个路径来展开访谈。想了解下,康辰在科研管理方面遇到的挑战有哪些?这个问题,请质量部总监张总来谈谈。
张宇总监:好的。在研发信息化建设之前,康辰在科研管理方面遇到的难题,主要体现在以下5个方面:
1、如何高效管理项目: 由于大部分研发人员都会同时承担多个研发项目,在项目管理过程中如何有效调配资源,如何提升员工工作效率,如何进行科学准确的绩效考核。
2、实验过程如何合规:研发一线实验员面临每天要抄录大量的研发实验数据,填写大量的原始记录,色谱数据计算错误率高,而且查找和统计效率低下。
3、如何做好风险管控:新药研发项目周期长、高投入、高风险等特点,如何规避风险、提高开发效率、加强新药开发过程中的管理,以便充分利用有限资源,在尽可能短的时间内,开发出高质量产品。
4、如何提高研发质量:研发实验工艺变更频繁,如何评估变更的风险,合规的文件管理、有效的偏差管控和CAPA跟进,如何把质量管理和研发过程有机结合,如何提高研发人员的质量规范水平。
5、如何有效节约成本:研发实验过程中因化学试剂名称复杂,名称众多,查找困难,经常发生库中明明有试剂却找不到,还存在台账与库存严重不符的情况,这经常导致研发人员想要的试剂找不到,或者周期很长;研发人员会每次大量申领试剂,以保障研发进度,但这会导致库房中大量试剂过期报废,研发员大量领用而浪费。
主持人:张总是站在业务的角度谈遇到的难题,相信这也是很多药企会遇到的很实际的共性问题,感谢张总的分析。信息化建设的价值就在于实现业务的需求,请李总分享下,康辰的信息化建设历程是怎样的?
李博总监:好的。我从科研管理系统的建设原则、建设路线、建设历程三个方面来谈这个问题。
建设原则:
1、总体规划,定期更新,分步实施:将科研管理系统分为项目管理、实验管理和质量管理三个方向规划设计,通过电子化流程具体制定落地措施;同时国内制药法规变化较大,规划必须跟得上法规的变化,因此规划一定要定期更新。
2、平台集中化,避免多系统集成:项目管理计划内容和实验管理结果反馈密切关联,质量管理又覆盖整个研发过程,因此科研管理系统一定要将平台集中,避免内部做多系统集成,以保证数据打通质量、规避验证风险。
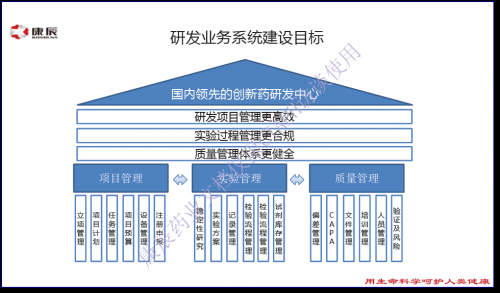
建设路线:
整体项目分为三期建设:
一期:2017-2019,科研管理系统和临床管理系统作为临床前和临床阶段的主要业务系统先期建设,而项目管理和质量管理作为科研管理系统第一阶段的主要内容进行开发,实现在研发横向上的项目管理和质量管理有机结合;实验管理作为科研管理第二阶段的主要内容,实现研发向下延伸到实验过程管理的合规、高效。
二期:2020-2021,完成注册申报系统建设、生产质量管理系统建设(QA&QC)和研发科研管理系统同平台建设,并完成科研管理系统和生产相关系统工艺交接信息的对接。
三期:完成研发端业务系统与管理系统数据打通(和ERP、eCTD、eDMS等集成),成为国内研发信息化领军代表。
建设历程:
科研管理系统建设从2016年12月份启动,当时国内研发实验室管理系统并不常见,而且系统建设思路是偏项目管理型,以项目管理系统PMS为主,实验记录功能不做电子化处理,后期根据实验室的需求再增加ELN系统做集成,但是这样做从合规角度来说无形中增加了验证风险。
鉴于以上背景,我们经过和研究院业务专家的密切沟通,先梳理出来研发实验室管理的三大需求:项目管理、实验管理和质量管理。项目管理系统功能相对简单,如果选择PMS软件平台,后期扩展性严重不足,同时实验管理和质量管理从技术难度到合规性要求很高,因此最终我们决定选择Lims平台作为基础平台,然后再进行实施方的选择。
经过近半年的产品交流和筛选,考虑到国内品牌产品只适用于QC实验室环境、实施人员研发业务知识相对欠缺、合规性也很差等因素,因此,选型只考虑国外产品,创腾和三维两家实施公司最终入围。由于两家公司的解决方案差异很大,为了使产品选型和需求贴合度更高,我们采取了产品试用的形式,经过近半年的产品试用,最终确定选择了三维作为系统实施方。
主持人:感谢李总的细致介绍,从建设原则、路线、历程三个层面分享了科研管理系统的建设。每一个项目实施过程中都会遇到很多实际的问题,请李总介绍下,科研管理系统建设中遇到了哪些挑战,也请介绍下应对策略。
李博总监:好的,来总体谈一下,我们在项目建设过程中遇到的挑战以及应对建议:
研发因品种不同差异性很大,没有标准化产品,和QC实验室解决方案完全不同。
研发实验室系统选型合规和功能同样重要,选系统和实施方也同等重要。
尽可能同平台,少集成,减少验证风险。
研发系统规划要和研发业务方向一致,切勿过渡考虑性价比忽视风险。
业务需求梳理一定要完整,形成详细的需求分析文档,我们通过对比两家公司方案编写出500条URS细节,此举为后期功能对比奠定了基础。
研发因涉及变更较多,一定要在业务部门培养一名偏业务管理的系统管理员,和IT系统管理员同步进行运维工作。
主持人:相信李总刚才分享的这些问题及应对策略,是实践中非常重要的方面。刚才介绍了科研管理系统的建设,落地后的效果是怎样的,请张总来介绍下。
张宇总监:好的。康辰的科研管理系统一期目前已经上线,取得了初步的效果:
1、研发信息系统的功能,包括研发立项管理、计划管理、项目进度管理、成果管理、研发物资管理、研发方案设计、研发试验记录、分析检测过程等,集多方面管理于一体,实现了研发项目的规范化、科学化、信息化管理,并从进度控制、执行调度、质量控制、成本控制等多个角度加强监控,以达到提高研发和项目管理效率的目标。
2、加强对研发过程的管理,实现研发过程的制剂设计、生产工艺优化、试验分析,以及试产、合成工艺调整等环节的全面管理。建立规范、高效的研发管理模式,提高研发过程的管理水平,从而提高新产品的开发速度,保持研究院良好的发展态势,增强核心竞争力。
3、提高研发实验工作的规范化程度,避免人工操作的随意性,使各项检验工作具有可溯源性,实现与分析检验业务密切相关的研发实验室人(人员)、机(仪器)、料(检品、材料)、法(方法)、环(环境、通讯)的全面资源管理。
4、通过仪器数据的自动采集,以及信息的自动调用、自动计算、自动查错,提高研发业务处理的自动化程度,提升工作效率,减少因人工操作而产生的差错,确保研发实验室数据的准确性、可溯源性,以及最大限度的无纸化。
5、实现研发数据的信息化管理,实现检验报告、研发报告及各种统计报表的自动生成,以及灵活、方便的查询功能,从而提高技术人员的工作效率,为领导管理与决策提供数据支持。
主持人:好的,感谢张总给出的效果分享,也非常感谢两位的倾情分享。CIAPH的价值在于搭建药企同仁之间的交流和互动平台,在康辰药业科研管理系统的分享内容里,应该有很多制药企业共性的场景,相信群内伙伴会有一些实际问题想要与李总、张总交流互动。下面是互动时间,欢迎大家踊跃发问。
互动问答环节
提问:您介绍的以上功能,是通过LIMS平台实现的吗?研发人员每天需进行的信息输入大概工作量有多大?
李博总监:主要功能都是通过Lims平台实现的,研发人员录入的信息量主要是申报资料和实验记录,申报资料目前功能涉及是Lims文件管理和eCTD撰写工具结合,做文档发布,但因为eCTD规范刚出台,此功能放到二期来做,还未实施。
张宇总监:系统平台中目前涉及工作量方面最大的是实验记录的填写,研发实验记录工作量主要看研发的项目情况,仿制药和创新药肯定是不一样的,不同的项目要求不同,实验要求自然也不同,虽然工作量较大,但是电子记录支持自动计算,下拉菜单,自动筛选等功能,工作量肯定要比纸质记录小很多。
提问:有集成ELN系统吗?
李博总监:我们目前的实验记录通过Lims平台就可以实现,但是复杂的实验必须要有ELN;Lims平台功能差异化也很大,很多Lims平台也自带ELN,具体需求还是要看实验的要求,不同的项目,设计实验过程是不一样的,要求也自然不同。
提问:前面提到的500条的URS,是IT部门主写的还是业务部门主写的?
李博总监:我给您一些经验,您可以按照这个流程来,第一步,IT和业务部门要先和供应商交流,深刻了解其功能,深刻了解系统功能才能具备编写URS的能力;第二步,通过交流选择几个需求匹配的产品厂家提供URS模板,此举既可以考察他们的能力,又可以提供足够的素材,这一步目的是为了更深刻的比较系统差异;第三步,将URS目录进行分类,IT写系统相关需求,业务部门分模块写各模块业务需求;第四步,项目组内部评审,防止模块间需求遗漏。做了这四步工作,不仅URS写出来了,同时大家对系统的了解也足够深刻了,选型自然也就有了结果。
提问:因为研发过程的灵活性,电子实验记录会不会受到局限?是不是要设计很多流程模板?
张宇总监:上系统前要先考虑管理的梳理,管理梳理健全后再考虑系统如何实现。研发有灵活性需求,但是电子记录可以根据需求来设计满足这种灵活性。模板肯定要设计,纸质记录也要设计的。
提问:电子实验记录的后台修改路径是否存档?这是否是实验合规性的证据?
李博总监:不管在Lims里面写实验记录,还是在ELN里面写记录,系统化管理肯定是要把数据存到数据库中,在系统建设完肯定要做验证,验证来证明功能设计能满足业务需求,因此个人认为,系统化管理肯定是能满足合规性的要求的。
提问:对于突发事件(比如断电)如何保证数据的及时记录?
李博总监:这个应该是系统设施的问题。一般来讲,突然事件有两种:第一种,数据采集客户端故障(类似于色谱工作站),这种情况数据肯定无法及时记录,采用网络版CDS能够记录最后一个数据采集点的数据,宕机时未保存记录无法找回;第二种,信息系统服务器故障宕机,这种情况本地的数据采集客户端依然在做实验,存储数据,服务器虽然宕机但是本地工作站软件一般都能缓存到本地最新的记录,等服务器恢复正常后本地工作站缓存的数据会自动传输给服务器,数据不会丢失。但是建议无论是工作站还是服务器均配备UPS,并且保证服务器硬件有容灾机制(集群、双机、数据备份系统、raid等安全措施),毕竟数据比硬件要有价值的多。
提问:申报资料的撰写是如何分工的?
李博总监:一般都是各专业负责人编写所负责模块的申报资料,这里提醒大家关注eCTD的发展,eCTD是将CTD模块化的资料电子化管理,支持多人协同、批注、浏览和验证,也是将单文件的申报资料模块化成为一个文件集合,未来也会带来文档管理的新需求。传统的文档管理系统是无法满足eCTD申报资料管理的,eCTD规范刚出,目前设计是文件管理对接eCTD撰写工具,但是可能会有调整,所以,还是需要及时关注CDE的相关政策要求。






